Por Fábio Ribeiro
•
10 de fevereiro de 2026
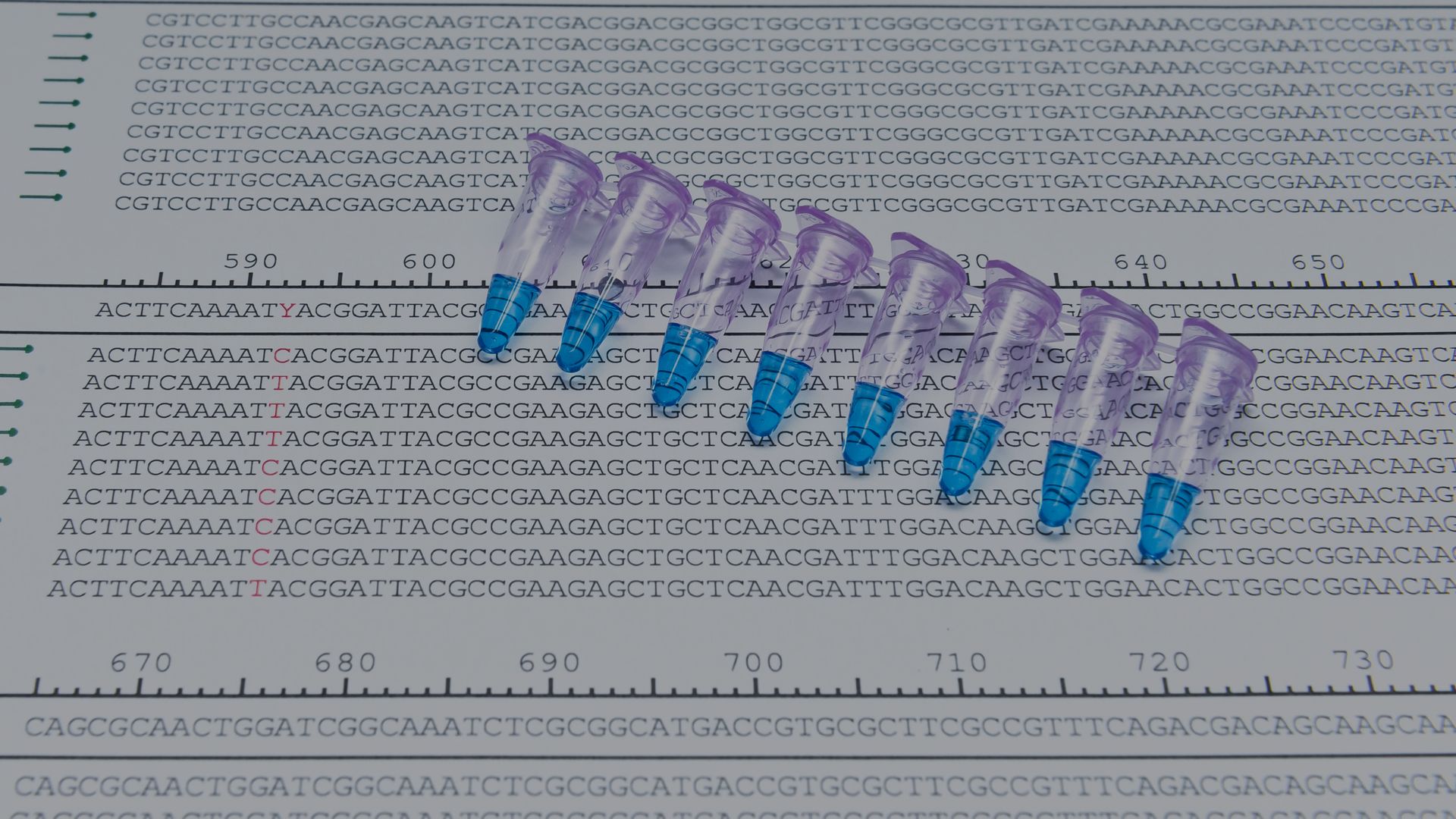
Durante mais de um século, a microbiologia dependeu fundamentalmente de uma ferramenta: a placa de Petri. Para estudar um microrganismo, precisávamos isolá-lo e cultivá-lo em laboratório. O problema? Descobrimos que estamos vendo apenas a ponta do iceberg. Estima-se que mais de 99% dos microrganismos do planeta não sejam cultiváveis pelas técnicas padrão. Vivíamos em uma ignorância parcial sobre a verdadeira diversidade microbiana da Terra e do nosso próprio corpo. A Metagenômica chegou para quebrar essa barreira. Ela é a ciência que estuda o material genético obtido diretamente de amostras ambientais, sem necessidade de cultivo prévio. Seja uma gota de água do mar, um grama de solo agrícola ou uma amostra intestinal humana, a metagenômica nos permite tentar ler o DNA de toda a comunidade ali presente. Neste artigo, vamos explorar as técnicas que revolucionaram a ciência, os desafios críticos de bancada que poucos mencionam e, crucialmente, emitir um alerta necessário sobre as armadilhas na interpretação clínica dos dados. O "Passo Zero": O Desafio Invisível da Extração de DNA Antes mesmo de pensarmos em sequenciar, enfrentamos o primeiro e talvez o maior obstáculo da metagenômica: extrair o DNA das células. Uma amostra ambiental (como fezes ou solo) é uma mistura caótica de organismos com estruturas muito diferentes. O Problema: Bactérias Gram-negativas rompem-se com facilidade. Já bactérias Gram-positivas (com paredes de peptidoglicano), esporos bacterianos, fungos (com paredes de quitina) e micobactérias são fortalezas difíceis de quebrar. O Viés da Extração: Se usarmos um método de extração muito suave (apenas químico), só veremos organismos frágeis. Se usarmos um método muito agressivo (como o bead-beating , que emprega microesferas e agitação mecânica intensa), conseguimos romper os organismos mais rígidos, mas corremos o risco de fragmentar excessivamente o DNA, o que prejudica certas análises posteriores (especialmente as de leituras longas). A escolha do kit e do protocolo de extração é fundamental e introduz o primeiro viés no estudo. Não existe um método universal perfeito; a escolha deve ser guiada pelo tipo de amostra e pela pergunta biológica. Como sempre na ciência, essas decisões precisam ser tomadas ainda na fase de desenho experimental, pois a bioinformática não fará milagres na etapa de análise. Uma boa decisão nesse momento pode ser a chave para controlar os vieses na interpretação dos resultados. A Caixa de Ferramentas: Como Estudamos o Invisível? Uma vez superado o desafio da extração, a metagenômica oferece diferentes estratégias de Sequenciamento de Nova Geração (NGS), cada uma com um propósito: 1. Sequenciamento de Amplicons (Ex.: 16S rRNA, ITS, ...) O Censo Demográfico: "Quem está aí?" Esta abordagem não sequencia tudo. Ela foca em amplificar (via PCR) genes marcadores específicos que funcionam como um "código de barras" molecular. Para bactérias, o alvo mais comum é o gene 16S rRNA ; para fungos, a região ITS . Vantagens: Custo mais baixo, lida bem com DNA um pouco mais fragmentado e é excelente para determinar a taxonomia (quem são os organismos) e a diversidade da comunidade. Limitações: Oferece pouca informação sobre a função real dos microrganismos e é "cega" para grupos que os primers não alcançam (ex.: um sequenciamento baseado em 16S bacteriano não detectará vírus). 2. Metagenômica "Shotgun" (Leituras Curtas) Análise Funcional: "Quem está aí e o que podem fazer?" Aqui, todo o DNA extraído é fragmentado aleatoriamente em pequenos pedaços (geralmente 150-300 pares de bases) e sequenciado, geralmente em plataformas Illumina. Vantagens: Revela o potencial funcional da comunidade. Podemos identificar genes de resistência a antibióticos, fatores de virulência e vias metabólicas complexas, além de detectar vírus e plasmídeos. Limitações: Custo elevado e bioinformática complexa. Montar genomas completos a partir de milhões de pequenos fragmentos, provenientes de centenas de espécies diferentes, é como tentar montar 500 quebra-cabeças diferentes, todos misturados na mesma caixa e com peças faltando. 3. Sequenciamento de Leituras Longas (Long-Read Sequencing) A Montagem de Genomas Completos Tecnologias como Oxford Nanopore e PacBio (HiFi) mudaram o jogo. Em vez de picotar o DNA em pedaços minúsculos, elas leem fragmentos gigantes (de milhares a dezenas de milhares de bases). Vantagens: Resolve o problema do quebra-cabeça. Com peças maiores, é muito mais fácil montar genomas completos de organismos não cultivados (os chamados MAGs - Metagenome-Assembled Genomes). É superior para detectar elementos móveis, genes de resistência completos e regiões repetitivas. Limitações: Geralmente tem um custo por base mais alto e, crucialmente, exige DNA de altíssima qualidade e alto peso molecular (HMW) na extração. Se a extração foi agressiva demais e quebrou o DNA, essa técnica não funciona bem. O Impacto Multissetorial da Metagenômica Ao nos permitir ler o DNA do ambiente, a metagenômica abriu portas em diversas áreas: Na Agricultura: Avaliar a saúde biológica do solo, identificar comunidades promotoras de crescimento e detectar fitopatógenos precocemente. Na Biotecnologia: Bioprospecção em ambientes extremos para identificar novas enzimas industriais (ex.: celulases, polimerases) ou novos compostos antimicrobianos escondidos no DNA de bactérias não cultiváveis. Na Medicina: O estudo do microbioma humano para o diagnóstico de infecções complexas, a compreensão de doenças inflamatórias e a influência da microbiota na resposta a medicamentos (farmacomicrobiômica). SEÇÃO CRÍTICA: O Dilema Clínico e o Alerta sobre a Interpretação Chegamos ao ponto mais delicado. O entusiasmo pelo microbioma humano gerou uma onda de estudos associando bactérias a praticamente todas as doenças conhecidas. Isso criou uma percepção perigosa de que um simples teste de microbioma pode diagnosticar condições complexas. Precisamos de cautela. A maioria dos estudos atuais são observacionais: eles mostram uma "foto" e identificam correlações, mas raramente provam causalidade. O Perigo da Confusão: Agente Etiológico vs. Bioindicador Vamos usar o exemplo crítico do câncer . Estudos mostram que certos tumores possuem uma comunidade bacteriana específica associada a eles. A pergunta que define tudo é: A galinha ou o ovo? 1. O Cenário do Agente Etiológico (Causa): Aquelas bactérias específicas causaram a inflamação que levou ao tumor? (Exemplo: H. pylori e câncer gástrico). Se sim, elas são alvos terapêuticos. 2. O Cenário do Bioindicador (Consequência/Oportunista): O tumor alterou o ambiente local (mudou o pH, nutrientes, oxigênio), criando um nicho perfeito para que certas bactérias "passageiras", que já estavam por perto, prosperassem? Nesse caso, elas são apenas um sinal de um ambiente doente, não a causa raiz. O Alerta da Biomelting: Interpretar a simples presença de um microrganismo como a causa de uma doença complexa, sem evidências mecanísticas, é um erro científico grave. Conclusão: Navegando na Complexidade A metagenômica é uma das ferramentas mais transformadoras da biologia moderna. No entanto, a transição desses dados para a prática exige rigor, que se estende da escolha do método de extração de DNA na bancada até a interpretação cuidadosa dos dados na bioinformática. Na Biomelting , entendemos que a metagenômica não é uma receita de bolo. Dominamos as técnicas de bancada para extrair o DNA difícil, as estratégias de sequenciamento (de amplicons a long-reads) e possuímos o olhar crítico para interpretar essa complexidade ecológica sem cair em armadilhas conceituais. Bibliografia Recomendada 1. O Desafio da Extração de DNA: Costea, P., Zeller, G., Sunagawa, S. et al. Towards standards for human fecal sample processing in metagenomic studies. Nat Biotechnol 35, 1069–1076 (2017). https://doi.org/10.1038/nbt.3960. 2. Visão Geral das Técnicas (Shotgun, Amplicons e Long-Reads): Quince, C., Walker, A., Simpson, J. et al. Shotgun metagenomics, from sampling to analysis. Nat Biotechnol 35, 833–844 (2017). https://doi.org/10.1038/nbt.3935. 3. O Poder dos Long-Reads na Metagenômica: Bertrand, D., Shaw, J., Kalathiyappan, M. et al. Hybrid metagenomic assembly enables high-resolution analysis of resistance determinants and mobile elements in human microbiomes. Nat Biotechnol 37, 937–944 (2019). https://doi.org/10.1038/s41587-019-0191-2. 4. Microbioma Humano e o Desafio da Causalidade (Crítico): Fischbach MA. Microbiome: Focus on Causation and Mechanism. Cell. 2018 Aug 9;174(4):785-790. doi: 10.1016/j.cell.2018.07.038. 5. Aplicações em Microbioma e Câncer (O dilema do "passageiro"): Sepich-Poore GD, Zitvogel L, Straussman R, Hasty J, Wargo JA, Knight R. The microbiome and human cancer. Science. 2021 Mar 26;371(6536):eabc4552. doi: 10.1126/science.abc4552. Erratum in: Science. 2024 Sep 27;385(6716):eadt2260. doi: 10.1126/science.adt2260.